Nosokomiale longûntstekking is de meast foarkommende en serieuze nosokomiale ynfeksje, wêrfan fentilator-assosjeare longûntstekking (VAP) 40% útmakket. VAP feroarsake troch refraktêre patogenen is noch altyd in lestich klinysk probleem. Jierrenlang hawwe rjochtlinen in ferskaat oan yntervinsjes oanrikkemandearre (lykas rjochte sedaasje, holleheffen) om VAP te foarkommen, mar VAP komt foar by maksimaal 40% fan pasjinten mei tracheale yntubaasje, wat resulteart yn langere sikehûsferbliuwen, ferhege gebrûk fan antibiotika en dea. Minsken binne altyd op syk nei effektiver previntyfmaatregels.
Ventilator-assosjeare longûntstekking (VAP) is in nije foarm fan longûntstekking dy't 48 oeren nei tracheale yntubaasje ûntstiet en de meast foarkommende en deadlike nosokomiale ynfeksje is op 'e intensive care-ienheid (ICU). De rjochtlinen fan 'e American Society of Infectious Diseases út 2016 hawwe VAP ûnderskieden fan 'e definysje fan sikehûsopnommen longûntstekking (HAP) (HAP ferwiist allinich nei longûntstekking dy't optreedt nei sikehûsopname sûnder in tracheale buis en net relatearre is oan meganyske fentilaasje; VAP is longûntstekking nei tracheale yntubaasje en meganyske fentilaasje), en de European Society en Sina binne fan betinken dat VAP noch altyd in spesjaal type HAP is [1-3].
By pasjinten dy't meganyske fentilaasje krije, farieart de ynsidinsje fan VAP fan 9% oant 27%, it mortaliteitssifer wurdt rûsd op 13%, en it kin liede ta ferhege systemysk antibiotikagebrûk, langere meganyske fentilaasje, langer ferbliuw op 'e IC, en ferhege kosten [4-6]. HAP/VAP by net-ymmúndefisjinte pasjinten wurdt meastentiids feroarsake troch in baktearjele ynfeksje, en de fersprieding fan mienskiplike patogenen en har resistinsjekarakteristiken fariearje mei regio, sikehûsklasse, pasjintpopulaasje en antibiotika-eksposysje, en feroarje yn 'e rin fan' e tiid. Pseudomonas aeruginosa dominearre VAP-relatearre patogenen yn Jeropa en Amearika, wylst mear Acinetobacter baumannii isolearre waarden yn tertiêre sikehûzen yn Sina. Ien tredde oant de helte fan alle VAP-relatearre deaden wurde direkt feroarsake troch de ynfeksje, wêrby't it mortaliteitssifer fan gefallen feroarsake troch Pseudomonas aeruginosa en acinetobacter heger is [7,8].
Troch de sterke heterogeniteit fan VAP is de diagnostyske spesifisiteit fan syn klinyske manifestaasjes, ôfbyldings- en laboratoariumtests leech, en it berik fan differinsjaaldiagnoaze is breed, wat it lestich makket om VAP op 'e tiid te diagnostisearjen. Tagelyk foarmet baktearjele resistinsje in serieuze útdaging foar de behanneling fan VAP. Der wurdt rûsd dat it risiko op it ûntwikkeljen fan VAP 3%/dei is tidens de earste 5 dagen fan gebrûk fan meganyske fentilaasje, 2%/dei tusken 5 en 10 dagen, en 1%/dei foar de rest fan 'e tiid. De peakinsidensje komt oer it algemien foar nei 7 dagen fan fentilaasje, dus d'r is in finster wêryn ynfeksje betiid foarkommen wurde kin [9,10]. In protte stúdzjes hawwe sjoen nei it foarkommen fan VAP, mar nettsjinsteande desennia fan ûndersyk en besykjen om VAP te foarkommen (lykas it foarkommen fan yntubaasje, it foarkommen fan re-intubaasje, it ferminderjen fan sedaasje, it ferheegjen fan it haad fan it bêd mei 30° oant 45°, en mûnlinge soarch), liket it foarkommen net ôfnommen te wêzen en bliuwt de assosjearre medyske lêst tige heech.
Ynhalearre antibiotika wurde sûnt de jierren 1940 brûkt om groanyske luchtwei-ynfeksjes te behanneljen. Omdat it de levering fan medisinen nei it doelgebiet fan ynfeksje (d.w.s. de luchtwei) maksimalisearje kin en systemyske side-effekten ferminderje kin, hat it in goede tapassingswearde sjen litten by in ferskaat oan sykten. Ynhalearre antibiotika binne no goedkard troch de Amerikaanske Food and Drug Administration (FDA) en it Europeesk Medisynenagentskip (EMA) foar gebrûk by cystyske fibrose. Ynhalearre antibiotika kinne de baktearjele lading en de frekwinsje fan fergruttingen by bronchiektasis signifikant ferminderje sûnder de algemiene bywurkingen te ferheegjen, en hjoeddeistige rjochtlinen hawwe se erkend as earste-line behanneling foar pasjinten mei pseudomonas aeruginosa-ynfeksje en faak fergruttingen; Ynhalearre antibiotika tidens de perioperative perioade fan longtransplantaasje kinne ek brûkt wurde as adjuvante of profylaktyske medisinen [11,12]. Mar yn 'e Amerikaanske VAP-rjochtlinen fan 2016 hienen saakkundigen gjin fertrouwen yn' e effektiviteit fan adjuvante ynhalearre antibiotika fanwegen it gebrek oan grutte randomisearre kontroleare proeven. De Fase 3-stúdzje (INHALE) dy't yn 2020 publisearre waard, helle ek gjin positive resultaten (ynhalaasje fan amikacine-assistearre intraveneuze antibiotika foar Gram-negative baktearjele ynfeksje feroarsake troch VAP-pasjinten, in dûbelblinde, randomisearre, placebo-kontroleare, faze 3-effektiviteitsstúdzje, yn totaal 807 pasjinten, systemyske medikaasje + assistearre ynhalaasje fan amikacine foar 10 dagen).
Yn dizze kontekst hat in team ûnder lieding fan ûndersikers fan it Regionaal Universitêr Sikehûs Sintrum fan Tours (CHRU) yn Frankryk in oare ûndersyksstrategy oannaam en in troch ûndersikers inisjearre, multisintraal, dûbelblinde, randomisearre kontroleare effektiviteitsstúdzje (AMIKINHAL) útfierd. Ynhalearre amikacine of placebo foar VAP-previnsje waard fergelike yn 19 icus yn Frankryk [13].
In totaal fan 847 folwoeksen pasjinten mei invasive meganyske fentilaasje tusken 72 en 96 oeren waarden willekeurich 1:1 tawiisd oan ynhalaasje fan amikacine (N = 417,20 mg / kg ideaal lichemsgewicht, QD) of ynhalaasje fan placebo (N = 430, 0,9% natriumchloride-ekwivalint) foar 3 dagen. It primêre einpunt wie de earste episoade fan VAP fan it begjin fan 'e randomisearre tawizing oant dei 28.
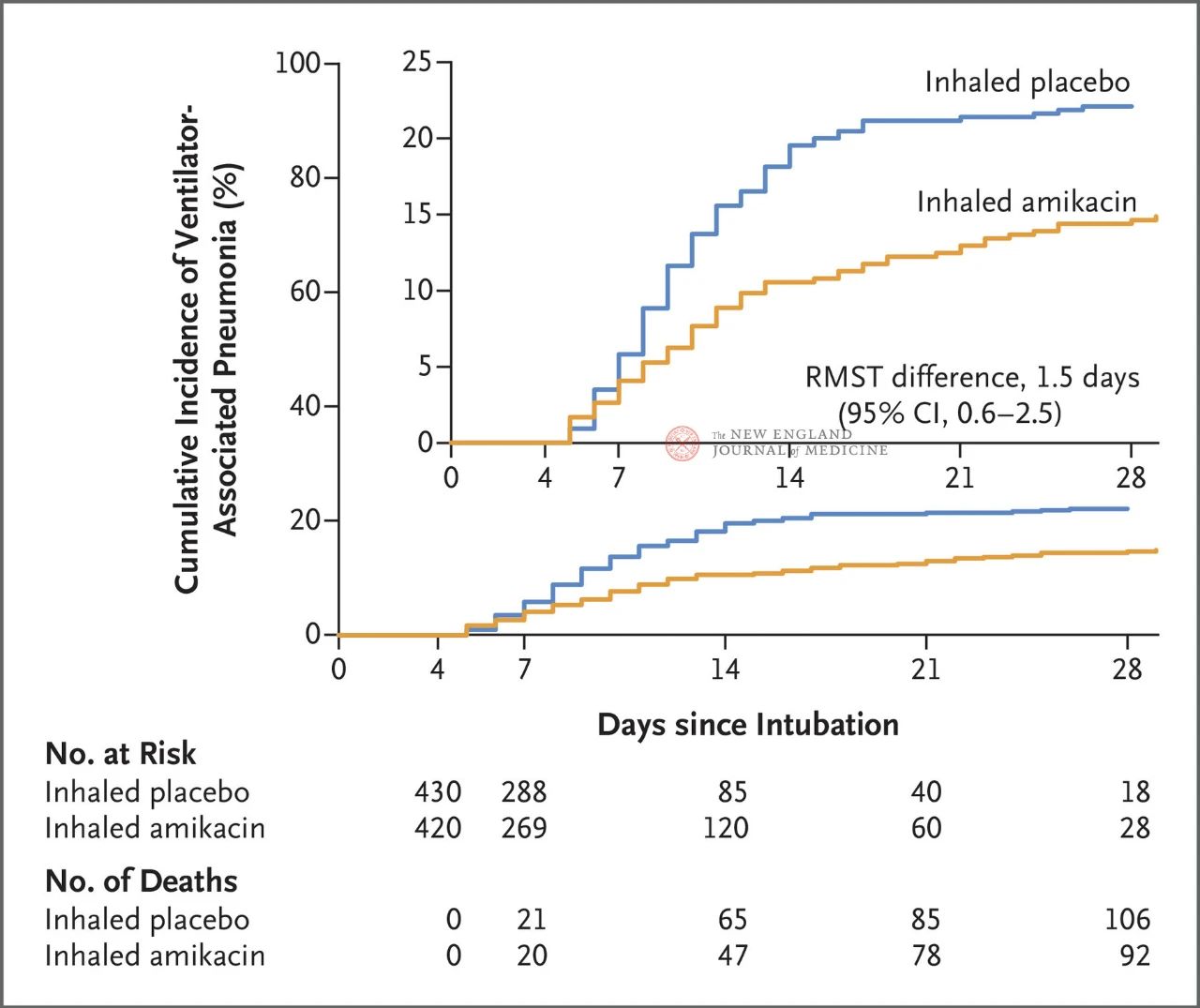
Resultaten fan 'e proef lieten sjen dat nei 28 dagen 62 pasjinten (15%) yn 'e amikacinegroep VAP ûntwikkele hiene en 95 pasjinten (22%) yn 'e placebogroep VAP ûntwikkele hiene (it beheinde gemiddelde ferskil yn oerlibjen foar VAP wie 1,5 dagen; 95% CI, 0,6~2,5; P=0,004).
Wat feiligens oanbelanget, ûnderfûnen sân pasjinten (1,7%) yn 'e amikacinegroep en fjouwer pasjinten (0,9%) yn 'e placebogroep serieuze neidielige effekten dy't relatearre wiene oan 'e stúdzje. Under dejingen dy't gjin akute nierskea hiene by randomisaasje, hiene 11 pasjinten (4%) yn 'e amikacinegroep en 24 pasjinten (8%) yn 'e placebogroep akute nierskea op dei 28 (HR, 0,47; 95% CI, 0,23~0,96).
De klinyske proef hie trije hichtepunten. Earst, wat it ûndersyksûntwerp oanbelanget, brûkt de AMIKINHAL-proef de IASIS-proef (in randomisearre, dûbelblinde, placebo-kontroleare, parallelle faze 2-proef mei 143 pasjinten). Om de feiligens en effektiviteit fan amikacine-fosfomycine-ynhalaasje-systemyske behanneling fan gram-negative baktearjele ynfeksje feroarsake troch VAP te evaluearjen) en de INHALE-proef om te einigjen mei negative resultaten, waarden lessen leard, dy't rjochte binne op it foarkommen fan VAP, en relatyf goede resultaten krigen. Fanwegen de skaaimerken fan hege mortaliteit en lange sikehûsopname by pasjinten mei meganyske fentilaasje en VAP, as amikacine-ynhalaasje signifikant ferskillende resultaten kin berikke yn it ferminderjen fan dea en sikehûsopname by dizze pasjinten, sil it weardefoller wêze foar de klinyske praktyk. Mei it each op de heterogeniteit fan lette behanneling en soarch by elke pasjint en elk sintrum, binne d'r lykwols in oantal betiizjende faktoaren dy't de stúdzje kinne bemuoie, sadat it ek lestich kin wêze om in posityf resultaat te krijen dat taskreaun wurdt oan ynhalearre antibiotika. Dêrom fereasket in suksesfolle klinyske stúdzje net allinich in poerbêst ûndersyksûntwerp, mar ek de seleksje fan passende primêre einpunten.
Twadder, hoewol aminoglykoside-antibiotika net oanrikkemandearre wurde as ien medisyn yn ferskate VAP-rjochtlinen, kinne aminoglykoside-antibiotika mienskiplike patogenen by VAP-pasjinten dekke (ynklusyf pseudomonas aeruginosa, acinetobacter, ensfh.), en fanwegen har beheinde opname yn longepitheelsellen, hege konsintraasje op it plak fan ynfeksje, en lege systemyske toksisiteit. Aminoglykoside-antibiotika wurde breed foarkar jûn ûnder ynademe antibiotika. Dit artikel is yn oerienstimming mei de wiidweidige skatting fan 'e effektgrutte fan intratracheale administraasje fan gentamicin yn lytse stekproeven dy't earder publisearre binne, wat mienskiplik it effekt fan ynademe aminoglykoside-antibiotika by it foarkommen fan VAP demonstrearret. It moat ek opmurken wurde dat de measte fan 'e placebo-kontrôles dy't selektearre binne yn' e proeven relatearre oan ynademe antibiotika normale sâltwetter binne. Mei it each op it feit dat atomisearre ynhalaasje fan normale sâltwetter sels in bepaalde rol kin spylje by it ferdunnen fan sputum en it helpen fan slijmoplossend middel, kin normale sâltwetter bepaalde ynterferinsje feroarsaakje yn 'e analyze fan' e stúdzjeresultaten, dy't wiidweidich beskôge wurde moatte yn 'e stúdzje.
Fierder is lokale oanpassing fan HAP/VAP-medikaasje wichtich, lykas antibiotikaprofylaxe. Tagelyk, nettsjinsteande de lingte fan 'e yntubaasjetiid, is de ekology fan 'e lokale IC de wichtichste risikofaktor foar ynfeksje mei multi-drug-resistente baktearjes. Dêrom moat de empiryske behanneling safolle mooglik ferwize nei de mikrobiologyske gegevens fan lokale sikehûzen, en kin net blyn ferwize nei de rjochtlinen of de ûnderfining fan tertiêre sikehûzen. Tagelyk wurde kritysk sike pasjinten dy't meganyske fentilaasje nedich binne faak kombineare mei multisysteemsykten, en ûnder de kombineare aksje fan meardere faktoaren lykas stresssteat kin der ek in ferskynsel wêze fan intestinale mikroben dy't oerprate nei de longen. De hege heterogeniteit fan sykten feroarsake troch ynterne en eksterne superposysje bepaalt ek dat de grutskalige klinyske promoasje fan elke nije yntervinsje in lange wei te gean is.
Pleatsingstiid: 2 desimber 2023